Niaj ĉefaj produktoj: Amina silikono, bloka silikono, hidrofila silikono, ĉiuj iliaj silikonaj emulsioj, plibonigiloj de frota rapideco kontraŭ malsekigo, akvorezistaj (sen fluoro, Karbono 6, Karbono 8), senmetalaj lavaĵkemiaĵoj (ABS, enzimoj, elastana protektilo, mangana forigilo), pliajn detalojn bonvolu kontakti: Mandy +86 19856618619 (Whatsapp)
Enkonduko al surfaktantoj
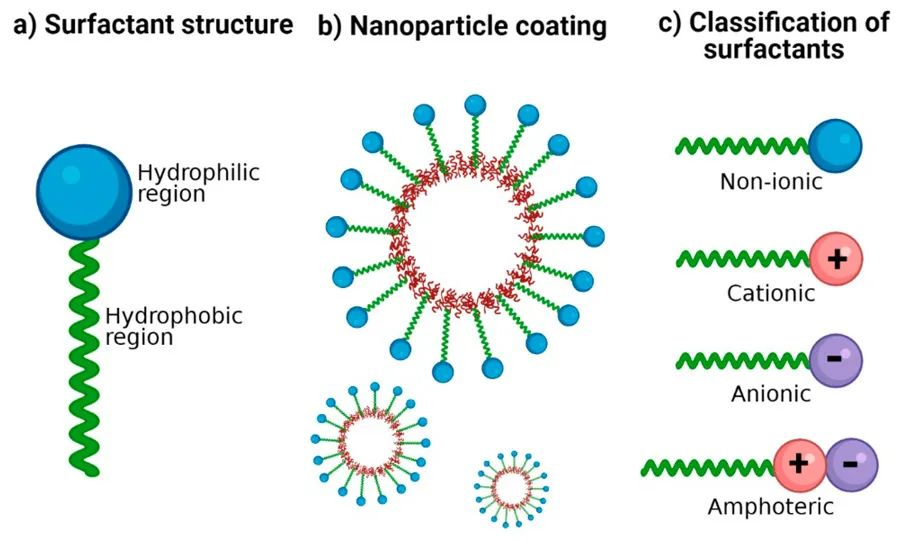
Surfaktantoj posedas amfifilan molekulan strukturon: unu fino enhavas hidrofilan grupon, nomatan la hidrofila kapo, dum la alia fino enhavas hidrofoban grupon, nomatan la hidrofoba vosto. La hidrofila kapo permesas al surfaktantoj dissolviĝi en akvo en sia monomera formo.
La hidrofila grupo ofte estas polusa grupo, kiu povas esti karboksila grupo (-COOH), sulfonacida grupo (-SO3H), amino-grupo (-NH2), aminoj kaj iliaj saloj, hidroksilaj grupoj (-OH), amidaj grupoj, aŭ eteraj ligiloj (-O-) kiel aliaj ekzemploj de polusaj hidrofilaj grupoj.
La hidrofoba grupo estas tipe nepolusa hidrokarbona ĉeno, kiel ekzemple hidrofobaj alkilaj ĉenoj (R- por alkilo) aŭ aromaj grupoj (Ar- por aril).
Surfaktantoj povas esti kategoriigitaj en jonajn surfaktantojn (inkluzive de katjonaj kaj anjonaj surfaktantoj), ne-jonajn surfaktantojn, amfoterajn surfaktantojn, miksitajn surfaktantojn, kaj aliajn. En surfaktantaj solvaĵoj, kiam la koncentriĝo de la surfaktanto atingas certan valoron, surfaktantaj molekuloj formas diversajn ordigitajn agregaĵojn konatajn kiel miceleoj. La procezo de miceliĝo, aŭ micelformado, estas decida fundamenta eco de surfaktantaj solvaĵoj, ĉar multaj gravaj interfacaj fenomenoj estas asociitaj kun la formado de miceleoj.
La koncentriĝo, ĉe kiu surfaktantoj formas miceleojn en solvaĵo, estas nomata la Kritika Micela Koncentriĝo (KMC). Miceloj ne estas fiksaj, sferaj strukturoj; anstataŭe, ili montras ekstreman neregulecon kaj dinamikajn formŝanĝojn. Sub certaj kondiĉoj, surfaktantoj ankaŭ povas montri inversajn miceleajn statojn.
Faktoroj Influantaj CMC:
- Strukturo de la surfaktanto
- Tipo kaj ĉeesto de aldonaĵoj
- Temperaturo
Interagoj Inter Surfaktantoj kaj Proteinoj
Proteinoj enhavas nepolusajn, polusajn kaj ŝargitajn grupojn, kaj multaj amfifilaj molekuloj povas interagi kun proteinoj laŭ diversaj manieroj. Depende de la kondiĉoj, surfaktantoj povas formi molekulorganizitajn agregaĵojn kun malsamaj strukturoj, kiel ekzemple miceleoj aŭ inversaj miceleoj, kiuj interagas malsame kun proteinoj.
La interagoj inter proteinoj kaj surfaktantoj (Proteino-Surfaktanto, PS) ĉefe implikas elektrostatikajn interagojn kaj hidrofobajn interagojn. Jonaj surfaktantoj interagas kun proteinoj ĉefe per la elektrostatikaj fortoj de la polusa grupo kaj la hidrofobaj interagoj de la alifata karbona ĉeno, ligante sin al la polusaj kaj hidrofobaj regionoj de la proteino, tiel formante PS-kompleksojn.
Ne-jonaj surfaktantoj ĉefe interagas kun proteinoj per hidrofobaj fortoj, kie la hidrofobaj ĉenoj interagas kun la hidrofobaj regionoj de la proteinoj. La interagado povas influi kaj la strukturon kaj la funkcion de la surfaktanto kaj la proteino. Tial, la tipo kaj koncentriĝo de surfaktantoj, kune kun la media kunteksto, determinas ĉu surfaktantoj stabiligas aŭ malstabiligas proteinojn, kaj ankaŭ ĉu ili antaŭenigas agregadon aŭ disperson.
HLB-Valoro de Surfaktantoj
Por ke surfaktanto montru sian unikan interfacan agadon, ĝi devas ekvilibrigi la hidrofobajn kaj hidrofilajn komponantojn. La HLB (Hidrofila-Lipofila Ekvilibro) estas mezuro de la hidrofila-lipofila ekvilibro de surfakantoj kaj servas kiel indikilo de la hidrofilaj kaj hidrofobaj ecoj de la surfakantoj.
La HLB-valoro estas relativa valoro (intervalante de 0 ĝis 40). Ekzemple, parafino havas HLB-valoron de 0 (neniu hidrofila komponanto), polietilen-glikolo havas HLB-valoron de 20, kaj la tre hidrofila SDS (natria dodecilsulfato) havas HLB-valoron de 40. La HLB-valoro povas servi kiel gvida referenco dum elektado de surfaktantoj. Pli alta HLB-valoro indikas pli bonan hidrofilecon, dum pli malalta HLB-valoro sugestas pli malbonan hidrofilecon.
Afiŝtempo: 10 septembro 2024

